
北京时候12月29日黎明,《新英格兰医学杂志》(NEJM)发表一项中国非劣效性3期飞快对照临床磨砺,其终端标明,关于有高危要素的轻中度Covid-19成东谈主患者,在至抓续临床康复时候方面,国产VV116非劣于Paxlovid(4天 vs. 5天;风险比,1.17;95%置信区间,1.02~1.36)跳蛋 露出,且不良事件更少。
这项磨砺由上海瑞金病院赵任阐述、上海仁济病院皋源阐述和上海瑞金病院宁光院士牵头,在7家上海病院开展,是omicron变异株流行时期首个针对Covid-19患者开展的国产口服抗病毒药物“头党羽”3期临床磨砺。VV116是由中国科学院上海药物权谋所与武汉病毒权谋所、新疆理化技艺权谋所等单元共同研发的一种新冠病毒RNA复制酶小分子禁绝剂。
这是NEJM发表的首个中国自主研发的新冠革命药临床磨砺,其在本年3—5月的上海极端心事时期高质地完成,尤为难能难得。《NEJM医学前沿》特邀药理学家、中国工程院院士丁健阐述和呼吸重症巨匠曹彬阐述区别从药理学和临床磨砺角度解读这项权谋。

VV116 vs. Paxlovid头党羽比较
——突发传染病高法度临床磨砺的重荷探索
王业明,曹彬*
中日友好病院呼吸与危重症医学科;国度呼吸医学中心;中国医学科学院呼吸病学权谋院
*通信作家
突发人人卫滋事件下开展临床磨砺自己就面领诸多心事,尤其是需要与疫情抢时候,在暴发窗口期完成新药的效用考证,最为要津的即是快!这么的临床磨砺终端将为后续该传染病再次暴发八成大流行提供枢纽的参考价值。
VV116是我国首个国产靶向新冠病毒RdRp的小分子药物禁绝剂。在2022年3至5月的上海疫情时期,权谋者快速筹划并开展了一项头党羽的非劣效性临床磨砺(ChiCTR2200057856,NCT05341609),当今该药物临床磨砺终端通过同业评议,于北京时候12月29日在《新英格兰医学杂志》(NEJM)上发表[1]。该权谋初度报谈了omicron流行情况下使用VV116和Paxlovid对高危要素的东谈主群症状改善时候的数据,不错为后续临床磨砺筹划以及临床用药陶冶提供枢纽参考价值。
为更好连络权谋初志和临床磨砺筹划,有必要先梳理一下那时临床磨砺的配景。率先,一系列高质地临床权谋接踵证明:小分子抗病毒药物molnupiravir(莫努匹韦;发病5天内)、Paxlovid(发病5天内)和瑞德西韦(发病7天内)早期使用,可减少具有高危要素东谈主群重症和示寂事件发生。这些临床磨砺主要集结在2020~2021时期,主要流行delta毒株,而且大无数受试者未接种新冠疫苗。
但在VV116权谋筹划时,有几个枢纽要素需要探讨:(1)上海的流行毒株为omicron BA.2,致病力较delta下落;(2)我国上海地区大部分东谈主群完成了疫苗接种;(3)Paxlovid照旧被我国CDE批准并被纳入卫健委诊疗决策,成为具有高危要素东谈主群法度抗病毒药物。权谋团队筹划了多中心飞快对照非劣效的临床磨砺,旨在评估VV116 vs. 对照药物(辉瑞Paxlovid)对轻型和鄙俚型具有高危要素的Covid-19患者的疗效。
出手临床主要至极竖立了转重和症状收复时候。权谋团队为了抢时候,和解了部分严谨性,包括未开展双盲筹划(因为双盲需要进行药品准备)。从磨砺经过文献,咱们不错发现VV116临床磨砺最终烧毁了双至极,仅保留了症状缓解时候这一个临床至极。可能是由于权谋团队在磨砺实行经过中发现omicron致病性下落,导致重症事件发生概率极低。也正如预期,终端标明两组进展为重型的受试者东谈主数为0。
也即是说,权谋团队并非胜利以症状改善时候动作临床至极,进行非劣临床磨砺筹划,而是原筹办以临床转重动作至极开展的非劣筹划。若何omicron致病性下落导致该至极无法竣事,权谋团队被动聘任症状改善动作至极。
最终VV116和Paxlovid组各招募384和387受试者。东谈主口学信息和基线情况终端标明仅有23.4%未接种新冠疫苗;92.1%属于轻型。主要至极(临床症状收复时候)终端标明,VV116 组中位症状收复时候为4 天,Paxlovid组症状收复时候为5天(风险比,1.17;95%置信区间,四房色播1.02~1.36)。家喻户晓,抗病毒药物距离发病的使用时候,是影响药物效果的要津要素。发病时候5天内使用抗病毒药物两组间无显着互异。按照年齿、疫苗、疾病严重进度、发病时候等要素进行亚组分析,终端均与全分析集(FAS)终端保抓一致,即VV116与Paxlovid在临床症状收复时候方面相等。病毒学终端是评估抗病毒药物十分枢纽的次要临床至极。在新冠病毒(鼻咽拭子)转阴方面,两组也保抓了相等的水平。
卡通色图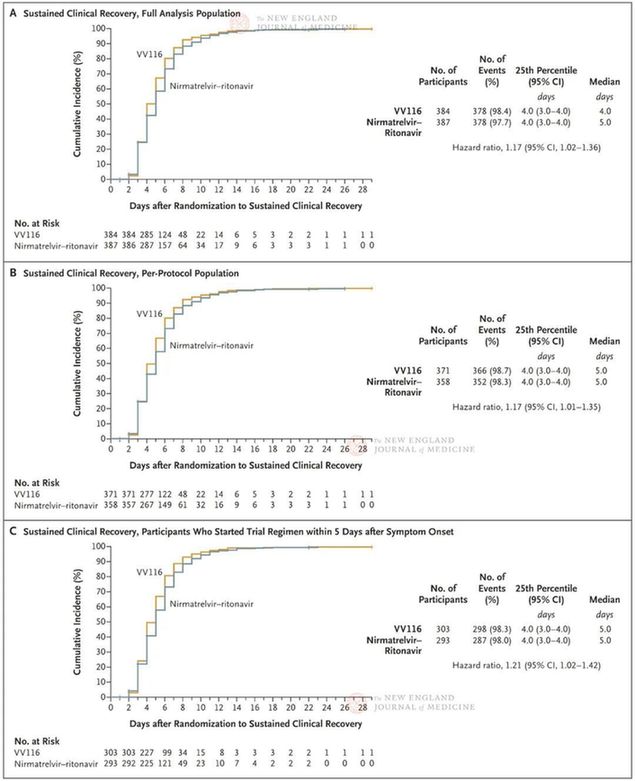
至症状收复时候
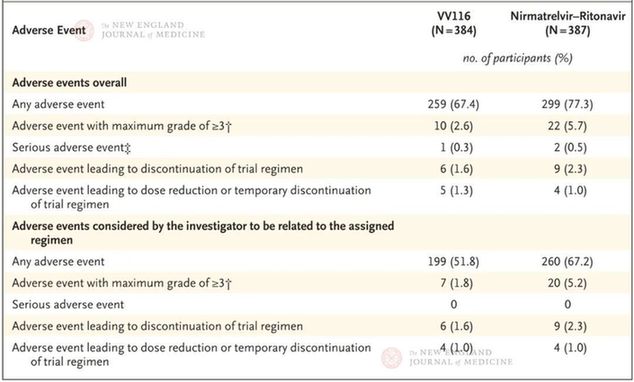
在安全性方面,VV116与Paxlovid也推崇出访佛细致的安全性,甚而在某些不良反映发生率方面低于Paxlovid,尤其是味觉禁绝。Paxlovid是奈玛特韦(3CL禁绝剂)和利托那韦(用于莳植血药浓度)的复合制剂,其中利托那韦因通过肝脏的CYP3A4酶代谢,与繁密药物存在相互作用(可具体参考确认书或使用确认)。对部分无法停用基础用药的患者十分未便。因此,在安全性和用药便捷性方面,VV116可能更为细致。
不良事件(安全性东谈主群)
从当今情况来看,靶向减少重症发生这一相宜证照旧基本不可能完成。针对新冠门诊轻症患者的症状改善相宜证,是当今尚未被炫耀的临床需求。由于流行毒株永恒在发生变化,相应的临床症状也出现了不同进度调动。好意思国FDA在2020年9月公布的Covid-19药物临床磨砺陶冶原则将14项症状动作主要至极,这是针对早期的新冠毒株症状。VV116权谋所给与的临床症状缓解修改为11个症状的缓解,未包含味觉禁绝、感觉禁绝、乏力/疲惫。
近期日本盐野义制药公司的抗新冠病毒新药ensitrelvir在日本获批,其在本年10月ISIRV-AVG的Webinar上共享临床磨砺终端也标明,倘若给与FDA公布的14项症状动作主要至极进行评估将弗成赢得阳性终端。而给与5项中枢症状抗病毒药物不错裁减病程约1天傍边,而且针对每一项症状评分也赢得疏导的获益。因此,连接变化的外部环境不仅是VV116权谋团队需要面对的,对其他新药临床磨砺团队亦然一个首要锻练。
临了,在面对疫情首要压力下,仍坚抓高法度开展新药临床磨砺的心事可思而知,咱们向整个在疫情时期开展严谨科学权谋的团队和受试者及家属示意敬意,感谢他们为新冠患者诊疗跳动所作念的接力,连接积贮可靠循证依据,保险患者的临床获益。
【VV116的药理学特质】
点评东谈主:中国科学院大学药学院阐述丁健院士
抗新冠病毒药物是灵验搪塞疫情的枢纽技巧之一,尤其是我国在疫情灵验防控取得积极首要效率的基础上,出台二十条优化步调解疫情防控新十条,实施疫情愈加科学精确防控,愈加需要加强抗新冠药物的研发、坐褥和储备。口服小分子抗新冠病毒药物具有使用便捷、可及性好等方面的上风,将在刻下和今后疫情防控中阐扬枢纽作用。
这项由上海瑞金病院赵任阐述、上海仁济病院皋源阐述和上海瑞金病院宁光阐述牵头,7家来自上海的病院参与的“VV116与奈玛特韦-利托那韦口服治愈Covid-19比较”的临床权谋终端标明,VV116与帕罗韦德(Paxlovid,奈玛特韦-利托那韦)对比,在患者抓续临床收复时候、病毒核酸转阴等方面,VV116均非劣于Paxlovid,且不良事件的发生率低于Paxlovid [1]。
VV116是中国科学院上海药物权谋所与中国科学院武汉病毒权谋所、中国科学院新疆理化技艺权谋所等单元共同研发的一款新式口服核苷类抗新冠病毒小分子药物。VV116研发团队照旧发表的部分临床前权谋终端标明[2],VV116的核苷三磷酸神志能浓度依赖地禁绝新冠病毒RNA复制酶(RdRp)的活性,IC50约为0.67 μM;在Vero E6细胞模子中,VV116推崇出较强的禁绝新冠病毒原始毒株复制的活性,EC50约为0.35 μM;在感染新冠病毒的小鼠模子中,VV116经口给药50 mg/kg,一天两次,一语气5天,可灵验破除病毒。此外,VV116在omicron变异株上也袒露了灵验的抗病毒活性,EC90约为0.64 μM [3]。
临床前权谋终端还标明,VV116安全性细致,且Ames磨砺、染色体畸变磨砺及体内骨髓微核磨砺终端均为阴性,无遗传毒性风险[2,4]。在国内完成的三项1期临床权谋中,单次给药剂量最高达1200 mg、屡次给药剂量最高达600 mg(一天两次,一语气5.5天)。这些磨砺终端标明,VV116安全性细致,未不雅察到严重的三级以上的不良事件(AE)[4]。
RNA复制酶动作病毒转录复制的中枢组件,是抗新冠病毒药物研发的枢纽靶标之一,且其功能在病毒变异中高度保守,针对此靶标研发的抗新冠病毒药物不易受病毒变异的影响。临床前权谋和1期临床权谋,照旧确证了VV116抗新冠病毒的活性和安全性[2-4],该项VV116与Paxlovid口服治愈Covid-19比较的临床权谋,进一步考证了VV116治愈omicron变异株感染患者的灵验性和安全性。
比较口服VV116和奈玛特韦-利托那韦治愈Covid-19的磨砺
VV116 versus Nirmatrelvir–Ritonavir for Oral Treatment of Covid-19
Cao Z, Gao W, Bao H, et al.
DOI: 10.1056/NEJMoa2208822
摘 要
配景
奈玛特韦-利托那韦已在多个国度赢得治愈Covid-19的伏击使用授权。但当今供应量低于全球需求量,因此有必要研发需要更多治愈决策。VV116是对SARS-CoV-2具有强效活性的口服抗病毒药。
门径
咱们在SARS-CoV-2 B.1.1.529(omicron)变异株引起疾病暴发时期开展了一项3期、非劣效性、不雅察者设盲的飞快磨砺。进展风险高的有症状轻度至中度Covid-19成东谈主患者被分拨接纳5天VV116或奈玛特韦-利托那韦治愈。主要至极是铁心第28天时,至抓续临床康复的时候。抓续临床康复的界说为整个Covid-19联系见解症状减弱至每项症状总分一语气2天为0或1分(限度为0~3分,评分较高示意症状较严重;11项量表的总分限度为0~33分)。淌若风险比的双侧95%置信区间下限大于0.8,则觉得证明非劣效性(风险比大于1示意VV116组至抓续临床康复的时候比奈玛特韦-利托那韦组短)。
终端
统统822名参与者接纳了飞快分组,771东谈主接纳了VV116(384东谈主)或奈玛特韦-利托那韦(387东谈主)。在至抓续临床康复的时候方面跳蛋 露出,VV116与奈玛特韦-利托那韦比拟的非劣效性在主要分析中得到证明(风险比,1.17;95%置信区间[CI],1.01~1.35),并在最终分析中得以保管(中位数,VV116组4天,奈玛特韦-利托那韦组5天;风险比,1.17;95% CI,1.02~1.36)。在最终分析中,在至症状抓续消退的时候(11项Covid-19联系见解症状中,每项一语气2天为0分)和至SARS-CoV-2检测初度呈阴性的时候方面,两组之间无显着互异。铁心第28天,两组均无参与者示寂或进展至重症Covid-19。VV116组的不良事件发生率低于奈玛特韦-利托那韦组(67.4% vs. 77.3%)。
论断
在有进展风险的轻度至中度Covid-19成东谈主患者中,在至抓续临床康复的时候方面,VV116不劣于奈玛特韦-利托那韦,何况安全性问题很少。(由苏州旺山旺水生物医药有限公司等资助;在ClinicalTrials.gov注册号为NCT05341609;在中国临床磨砺注册中心注册号为ChiCTR2200057856。)